covid-19, vacunas
La pandemia de COVID-19 no ha terminado. No pasará simplemente porque nos hemos cansado de él. Pero es igualmente erróneo pensar que no estamos mejor ahora que durante los primeros días de 2020.
20 diciembre 2022.- Los últimos tres años han producido una inmensa cantidad de investigación y un análisis cuidadoso del SARS-CoV-2. Esta creciente base de conocimiento nos ha permitido desarrollar vacunas y medicamentos antivirales efectivos para combatir la propagación del virus. Aún así, esto no justifica la autocomplacencia: nuestras vacunas actuales no son infalibles, la inmunidad disminuye. Necesitamos seguir avanzando, desarrollando tecnología de vacunas de próxima generación que brinde inmunidad duradera y ampliamente neutralizante.
Inmunidad menguante: infección, enfermedad grave y hospitalización
El estándar de oro para cualquier vacuna es la protección contra la adquisición de infecciones: si no puede infectarse, no puede enfermarse. Pero para la mayoría de los virus respiratorios, esta es una barra alta para establecer. Enfermedades como la poliomielitis y el sarampión nos otorgan inmunidad "esterilizante" de por vida después de la infección. Por extensión, también lo hacen las vacunas que protegen contra ellos. Pero a diferencia de la poliomielitis o el sarampión, la infección por un virus respiratorio no nos proporciona una inmunidad duradera.
Esta es la razón por la que, por ejemplo, tenemos temporadas anuales de gripe, y las reinfecciones son comunes. La inmunidad inducida por la vacuna disminuye en consecuencia. COVID-19 no es una excepción.
Datos recientes de Qatar sugieren que las infecciones pre-omicron son solo un 35,5% efectivas para proteger contra la reinfección sintomática con las subvariantes BA.4 o BA.5. Esta cifra se desploma al 27,7 % cuando también se tienen en cuenta las infecciones asintomáticas. Y para que quede más claro, también se ha documentado la reinfección con la misma variante.
Muchos esperaban que la inmunidad contra la infección se desvaneciera. La esperanza era que se mantuviera la inmunidad contra enfermedades graves y la hospitalización. En este escenario, aquellos que recibieron un curso "completo" de la vacuna, generalmente entendido como dos dosis de cualquiera de las vacunas de primera generación, aún serían susceptibles a la infección, pero solo sería una infección leve.
Un nuevo informe publicado por los Centros para el Control y la Prevención de Enfermedades (CDC) de EE.UU. sugiere lo contrario.
Los investigadores de los CDC recopilaron datos a través de la red Influenza and Other Viruses in the Acutely Ill (IVY), que consta de 21 hospitales grandes repartidos en 20 ciudades diferentes en 18 estados. Fundado en 2019, el propósito inicial de IVY era rastrear la efectividad de la vacuna contra la influenza entre los pacientes ingresados en la unidad de cuidados intensivos (UCI). Tras el brote de COVID-19, la iniciativa se amplió para inscribir también a pacientes hospitalizados con COVID-19. Su último análisis se basa en un grupo de 4730 pacientes adultos inmunocompetentes inscritos entre el 26 de diciembre de 2021 y el 31 de agosto de 2022.
Luego, los pacientes inscritos se dividieron en cuatro grupos diferentes, según su estado de vacunación: 1) aquellos que no habían sido vacunados antes de contraer el virus, 2) aquellos que habían recibido dos dosis de las vacunas originales de ARNm al menos catorce días antes de contraer el virus. , 3) aquellos que recibieron dos dosis más una dosis de refuerzo de las vacunas originales de ARNm al menos siete días antes de la aparición de la enfermedad, y 4) aquellos que recibieron dos dosis más dos dosis de refuerzo de las vacunas originales de ARNm, nuevamente al menos siete días antes de la enfermedad comienzo.
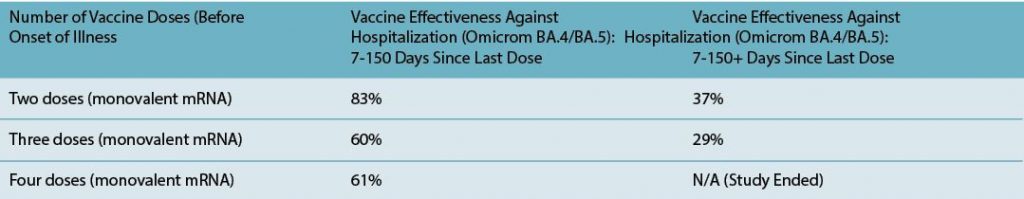
El equipo de científicos encontró que, en aquellos que recibieron dos dosis, la efectividad de la vacuna contra la hospitalización durante el período de predominio BA.1/BA.2 rondaba el 63%. Después de 150 días, la eficacia de la vacuna se redujo al 34 %. En el grupo que recibió dos dosis más una dosis de refuerzo, la efectividad de la vacuna contra la hospitalización comenzó en un 79 % antes de caer al 41 % después de 120 días (Tabla 1).

Efectividad de la vacuna contra la hospitalización durante la onda Omicron BA.1/BA.2, de 7 a 150 días desde la última dosis y más de 150 días desde la última dosis. Fuente: Acceso a la Salud Internacional.
Se observó una disminución similar de la protección contra la hospitalización durante la ola de infecciones BA.4/BA.5. Aquí, la eficacia de la vacuna en el grupo de dos dosis comenzó en un 83 %, pero se desplomó a solo un 37 % después de 150 días. Después de dos dosis y una vacuna de refuerzo, la eficacia de la vacuna se mantuvo en un 60 % antes de descender al 29 %. Y la eficacia de la vacuna después de dos dosis y dos inyecciones de refuerzo se mantuvo en aproximadamente el 60 % durante 120 días (Tabla 2).
El problema de la disminución de la inmunidad no es nuevo, pero nos obliga a reevaluar si nuestro enfoque actual de vacunación es el mejor.
¿Soluciones? Refuerzos y “vacunas universales”
En términos generales, las soluciones disponibles se pueden dividir en dos campos: a corto y largo plazo.
A corto plazo, las personas deberán continuar recibiendo sus refuerzos a intervalos de alrededor de cuatro a seis meses. Para los mayores de 55 años, debería estar más cerca de la marca de los cuatro meses. Parte de este enfoque es garantizar que los refuerzos se adapten para apuntar a la variante dominante en circulación.
Aunque todavía no tenemos una comprensión exhaustiva de los biomarcadores asociados con la protección inmunitaria, conocidos como "correlatos de protección", hay suficiente evidencia que sugiere que los títulos de anticuerpos neutralizantes juegan un papel clave. Estos anticuerpos se alojan en la proteína espiga y se unen a ella, evitando que el virus entre en nuestras células.
Cuanto mayor sea el número de anticuerpos neutralizantes, mayor será la protección contra la infección. Pero los niveles de anticuerpos neutralizantes comienzan a disminuir significativamente, hasta una disminución de cinco veces, dentro de los tres o cuatro meses posteriores a la vacunación. Y lo que es más importante, los altos niveles de anticuerpos neutralizantes son tan útiles como "precisos". Todos los anticuerpos del mundo no servirán de nada si no pueden unirse al antígeno relevante.
Es por esta misma razón que necesitamos actualizar nuestras vacunas contra la gripe todos los años, para asegurarnos de que los antígenos de la vacuna coincidan con los de las últimas cepas en circulación. Cuando ocurre una falta de coincidencia, terminamos con una temporada de gripe más severa. SARS-CoV-2 no es diferente.
Aunque todavía son escasos, los datos preliminares sobre las vacunas de refuerzo bivalentes aprobadas por la FDA indican que tener en cuenta este desajuste puede ayudar a reducir la capacidad del virus para evadir nuestro sistema inmunológico y causar daños graves. Un comunicado de prensa de Pfizer informa que las personas de 55 años en adelante disfrutaron de un aumento de cuatro veces en los niveles de anticuerpos neutralizantes contra Omicron BA.4/BA.5 en comparación con aquellos que recibieron una inyección de refuerzo de la vacuna original de ARNm de COVID-19. En comparación con los que no recibieron la vacuna de refuerzo, los títulos de anticuerpos neutralizantes un mes después de la vacunación fueron 13 veces más altos en adultos mayores de 55 años. Los adultos más jóvenes también vieron los beneficios, con un aumento de nueve veces en los títulos de anticuerpos.
Y en un estudio publicado en el servidor de preimpresión bioRxiv, los investigadores descubrieron que la vacuna de refuerzo bivalente también sigue siendo eficaz contra los miembros más nuevos de la familia Omicron, BA.2.75.2 y BQ.1.1.
¿La cuestión? Con el tiempo, la gente inevitablemente se cansará de necesitar dos o tres inyecciones de refuerzo al año. La aceptación de la vacuna disminuirá y volveremos al punto de partida. Está claro que debemos seguir mejorando nuestras vacunas contra el COVID-19 para que brinden una inmunidad amplia y duradera. Es más fácil decirlo que hacerlo, pero se están produciendo avances prometedores.
Dirigirse a regiones altamente conservadas del genoma viral
Una forma de lograr una amplia inmunidad resistente a variantes es apuntar a regiones altamente conservadas del genoma viral.
Las vacunas de ARNm actuales funcionan al exponer nuestros cuerpos a la proteína de punta del SARS-CoV-2, de la que depende el virus para unirse y eventualmente ingresar a nuestras células. Los anticuerpos que bloquean la proteína espiga pueden bloquear la infección. El problema es que la proteína espiga es propensa a la mutación: su estructura puede cambiar mucho sin sacrificar la funcionalidad. Por extensión, las vacunas basadas únicamente en la proteína de pico corren el riesgo de perder eficacia cuando se enfrentan a nuevas variantes.
La proteína de la nucleocápside es una proteína estructural con un papel integral en el ensamblaje viral y el empaquetamiento del material genético (Figura 1). Se conserva en un 90 % entre el SARS-CoV-1 y el SARS-CoV-2, en comparación con el 76 % de la proteína espiga. Estas dos características combinadas lo convierten en un objetivo muy prometedor para el diseño de vacunas.

A esto se suma el hecho de que se ha demostrado que la proteína de la nucleocápside provoca una poderosa respuesta de las células T. Mientras que las células B producen anticuerpos que pueden unirse a las partículas virales antes de que ingresen a las células, las células T se encargan de destruir las células huésped ya infectadas con el virus; cuanto más fuerte sea la respuesta de las células T, mejor podrá el cuerpo contener la propagación del virus y eliminar la infección. Los análisis de personas infectadas con SARS-CoV-1 han indicado que la inmunidad de las células T específicas de N puede ser muy duradera, y algunas personas conservan las células T de memoria hasta 17 años después de la infección inicial. Estas mismas células T lograron reconocer la proteína de la nucleocápside del SARS-CoV-2, montando una respuesta inmune rápida y específica.
De hecho, la investigación publicada en Science Translational Medicine corrobora esto, lo que sugiere que una vacuna de ARNm que se dirige tanto a la proteína de punta (S) del SARS-CoV-2 como a la proteína de la nucleocápside (N) puede ofrecer una protección más fuerte y más amplia que la actual, solo de punta. vacunas.
Hajnik et al. ratones separados en tres grupos: un grupo de control, que recibió una solución salina; un grupo de prueba, que recibió la vacuna bivalente mRNA-S+N; y un segundo grupo de prueba, que recibió una vacuna de ARNm que contenía solo la proteína de punta (ARNm-S). Las vacunas se administraron por vía intramuscular en dos dosis, una inicial y un refuerzo tres semanas después. Luego infectaron a los ratones con una cepa de SARS-CoV-2 adaptada a ratones dos semanas después de la administración de la vacuna de refuerzo. Hicieron lo mismo con los hámsters.
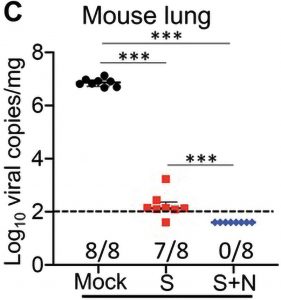
Tanto la vacuna mRNA-N+S como la vacuna mRNA-S lograron controlar con éxito la infección, casi sin virus infeccioso detectable en los pulmones (Figura 2).
Las vacunas también funcionaron bien contra el virus Delta en modelos de hámster, pero lo que es más importante, la vacuna mRNA-N+S superó a la vacuna de pico único. Mientras que la vacuna mRNA-S logró reducir las copias de ARN viral pulmonar 57 veces en comparación con el simulacro, la vacuna mRNA-S+N logró hacerlo 770 veces. Ambas vacunas protegieron contra el daño pulmonar, incluida la bronquiolitis y la neumonía intersticial.
Para probar más a fondo la amplitud de la respuesta inmunitaria provocada por la vacuna mRNA-N+S, Hajnik et al. hámsteres expuestos a la variante Omicron (BA.1). Con dos microgramos, la vacuna de pico único indujo una eliminación viral modesta de los pulmones; una reducción de 12 veces en las copias de ARN viral dos días después de la infección. La vacuna mRNA-N+S, por el contrario, logró eliminar completamente las copias de ARN viral de los pulmones el segundo día de la infección.
Lo mismo sucedió con los títulos virales, ya que cuatro de cada cinco hámsteres no tenían niveles detectables de virus infecciosos.
Más por menos: tecnología de ARN autoamplificador
Otro avance prometedor en la lucha contra la COVID-19 y sus múltiples variantes es la adopción de la tecnología de ARN autoamplificador.
Mientras que las vacunas tradicionales de ARNm de la COVID-19 se basan únicamente en la secuencia genética que codifica la proteína espiga del SARS-CoV-2, las vacunas de ARN autoamplificador incluyen una secuencia de ARN de alfavirus que codifica cuatro proteínas no estructurales. Una vez dentro de una célula huésped, estas proteínas no estructurales se unen para formar una molécula llamada ARN replicasa, una "fotocopiadora" transportable que imprime múltiples copias de la secuencia de ARNm (Figura 3). Esto significa que cada secuencia de ARN incluida en la vacuna puede hacer copias de sí misma, aumentando la cantidad de antígeno producido. También extiende la duración de la traducción del ARNm durante un período de tiempo más largo; El ARNm derivado de la vacuna generalmente se degrada después de uno o dos días, lo que limita la expresión de proteínas a dos o tres días como máximo. Sin embargo,
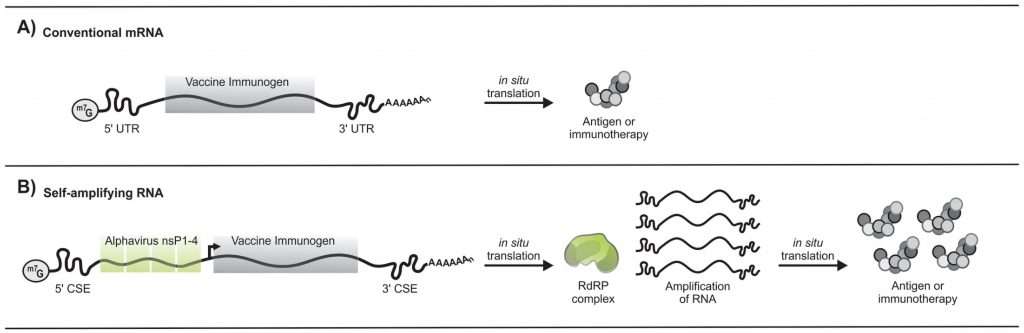
Los ARNm convencionales codifican el inmunógeno de la vacuna y las UTR 5' y 3' flanqueantes. Un antígeno o inmunoterapia se traduce del transcrito no replicante. B) El ARN autoamplificador codifica las secuencias CSE 5′ y 3′, los genes nsP1-4, un promotor subgenómico y el inmunógeno de la vacuna. Después de la traducción in situ, las proteínas nsP1-4 forman un complejo RdRP que reconoce las secuencias CSE flanqueantes y amplifica las transcripciones que codifican la vacuna. Esto da como resultado una acumulación del antígeno o inmunoterapia dentro de la célula. De: “Vacunas de ARN autoamplificador para enfermedades infecciosas” Bloom et al. 2020
La tecnología de ARN autoamplificador viene con una serie de beneficios. Por un lado, debido a que cada secuencia de ARN producirá múltiples copias de sí mismo, los fabricantes pueden usar una cantidad mucho menor por dosis de vacuna. La dosis más pequeña permite incluir múltiples cadenas diferentes de ARNm, cada una codificando su propio antígeno, en una vacuna. El enfoque de ahorro de dosis también reduce significativamente el costo de producción; el precio de la vacuna cae en consecuencia, haciéndola más accesible para las naciones de bajos y medianos ingresos.
Al igual que las vacunas de ARNm, la fabricación de ARN autoamplificador es completamente sintética. La fabricación no requiere crecimiento en ninguna célula viva. Es enteramente un proceso químico. La producción es rápida y flexible y se puede ajustar rápidamente para responder a las nuevas demandas. La infraestructura de fabricación y el control de calidad se simplifican enormemente en comparación con las vacunas tradicionales.
Dado que el ARNm autoamplificador permite que se produzca una mayor cantidad del antígeno objetivo durante un período de tiempo más largo, le brinda a nuestro sistema inmunitario una mejor oportunidad de aprender lo que necesita para desarrollar una respuesta inmunitaria altamente específica. Una exposición más prolongada a un antígeno permite que madure la respuesta de los anticuerpos, para producir anticuerpos neutralizantes más potentes y de mayor afinidad, así como anticuerpos que pueden provocar citotoxicidad celular. Además, una exposición más prolongada al antígeno es importante para generar células T de memoria necesarias para una memoria duradera.
Administración intradérmica: aumento de la inmunidad celular
La forma en que se administra una vacuna, a pesar de no ser parte de la vacuna per se, contribuye igualmente a la inmunogenicidad y seguridad de la vacuna. Esto incluye tanto el equipo como la vía de administración.
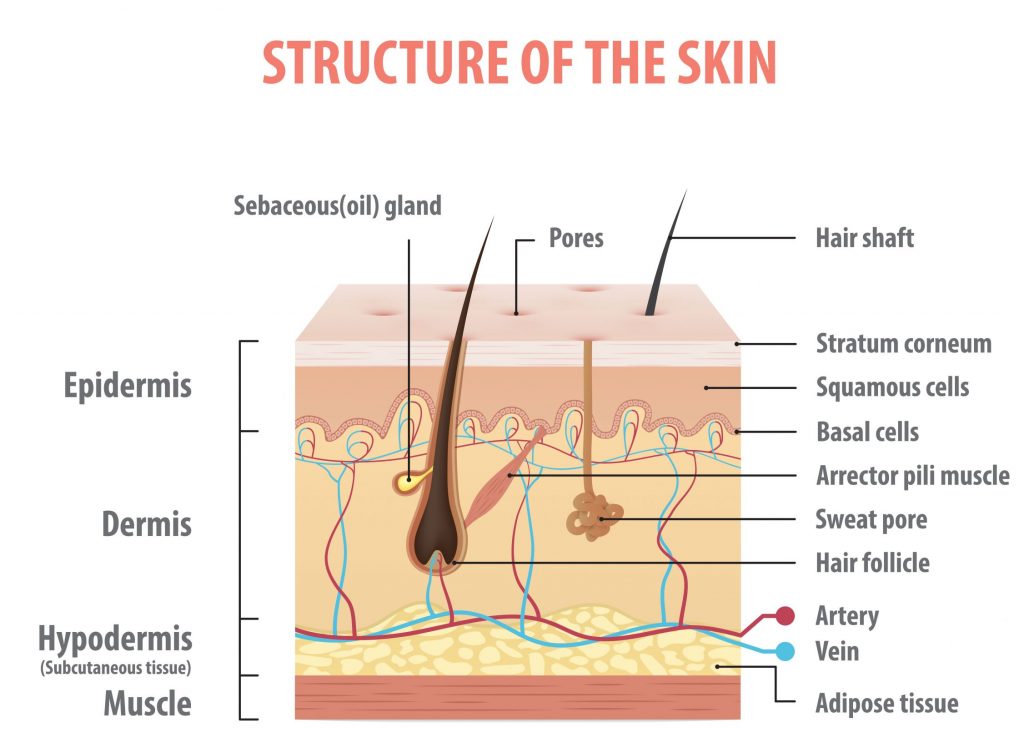
Nuestra piel se compone de tres capas: la capa protectora más externa llamada epidermis, una capa intermedia llamada dermis y una capa grasa en la parte inferior llamada hipodermis o tejido subcutáneo. La mayoría de las vacunas contra el COVID-19 se inyectan en el tejido muscular, que se encuentra muy por debajo de la piel. Este ha sido el enfoque estándar durante mucho tiempo. Pero la administración intradérmica tiene algunas ventajas distintas.
La capa de la dermis de la piel está repleta de células inmunitarias, incluidas las células presentadoras de antígenos (APC). Estos juegan un papel vital en la iniciación y modulación de nuestro sistema inmunológico, incluida nuestra respuesta inmune adaptativa. En particular, varios tipos diferentes de células dendríticas se adhieren a los antígenos y los presentan a las células T vírgenes, lo que ayuda a formar y madurar una respuesta inmunitaria celular específica. Dado que la inyección intradérmica permite que el antígeno se produzca muy cerca de estas células presentadoras de antígeno, puede dar lugar a una respuesta inmunitaria adaptativa más rápida y más precisa. Un estudio reciente que comparó la administración intradérmica e intramuscular del dominio de unión al receptor (RBD) del SARS-CoV-2 lo confirmó y describió respuestas mejoradas de las células T después de la inyección en la dermis.
La administración intradérmica viene con el beneficio adicional de las opciones de administración sin aguja, como los inyectores de chorro. Estos utilizan resortes o gas comprimido para producir una corriente estrecha de líquido a alta presión que penetra en la piel y administra la vacuna. La falta de una aguja ayuda a mejorar la aceptación, especialmente entre las poblaciones más jóvenes y reacias a las agujas. La entrega sin agujas también anula la posibilidad de reutilización de agujas y la posterior contaminación cruzada, que sigue siendo un problema común en muchas partes del mundo, con hasta 1,3 millones de muertes al año atribuidas a tales prácticas.
Y ahora qué hemos de esperar
Las vacunas de ARNm actuales funcionan bien, protegiendo contra infecciones y enfermedades graves, pero lo hacen solo por un período corto. Los niveles de anticuerpos comienzan a disminuir tan pronto como tres meses después de la vacunación, y con ellos disminuye la protección contra la inmunidad. Los datos de los CDC indican que la protección contra enfermedades graves y hospitalizaciones disminuye poco después, incluso contra variantes "más leves" como omicron.
El programa de vacunación debe adaptarse en consecuencia: para una protección óptima, se deben buscar dosis de refuerzo cada cuatro a seis meses. Los mayores de 55 años deben inclinarse hacia un intervalo de cuatro meses, los menores de 55 pueden salirse con la suya con un intervalo de seis meses. En ambos casos, la consistencia es clave.
Con suficientes fondos e investigación, estos refuerzos pueden eventualmente ser reemplazados por vacunas más duraderas y ampliamente neutralizantes. Las bases tecnológicas para esta transición están en desarrollo mientras hablamos, con avances en el diseño de antígenos, la expresión de antígenos y la administración de antígenos. Es importante destacar que estos factores no son mutuamente excluyentes: el progreso en uno se puede combinar con el progreso en otro, con los beneficios de cada uno "apilándose" uno encima del otro.
Aunque un optimismo cauteloso puede estar justificado, haríamos bien en recordar que desarrollar vacunas que induzcan inmunidad esterilizante (protección total contra la infección) es extremadamente difícil. A pesar de décadas de investigación sobre la influenza, por ejemplo, todavía carecemos de vacunas que ofrezcan tal protección contra los virus. El Virus de la Inmunodeficiencia Humana (VIH) es otro ejemplo; después de más de cuarenta años, todavía no tenemos vacunas exitosas. Pero la lucha contra el VIH demuestra que, incluso en ausencia de vacunas, se pueden lograr avances. Los medicamentos de profilaxis previa a la exposición (PrEP) ayudan a prevenir la infección en personas en riesgo de exposición, y el tratamiento antirretroviral (TAR) ayuda a quienes ya tienen el VIH a reducir los niveles a niveles apenas perceptibles, lo que les permite vivir una vida larga y saludable.
Puede ser necesaria una estrategia similar, que gire en torno a medicamentos antivirales altamente activos, para controlar COVID-19 mientras trabajamos en vacunas capaces de inducir inmunidad esterilizante.
Fuente: William R. Haseltine, PhD, es director y presidente del centro de estudios ACCESS Health International, ex profesor de la Escuela de Medicina y la Escuela de Salud Pública de Harvard y fundador de los departamentos de investigación del cáncer y el VIH/SIDA de la universidad. También es el fundador de más de una docena de empresas de biotecnología, incluida Human Genome Sciences































COMENTARIOS