Un escáner cerebral revela la extensión del daño causado por la enfermedad de Alzheimer. Fuente: Zephyr/Science Photo Library Los investig...
 |
| Un escáner cerebral revela la extensión del daño causado por la enfermedad de Alzheimer. Fuente: Zephyr/Science Photo Library |
Los investigadores buscan combinaciones de medicamentos, vacunas y terapia génica a medida que forjan la próxima generación de tratamientos para la afección.
04 abril 2023.- Cuando la neuróloga Reisa Sperling dio un paso adelante para recibir su premio a la trayectoria en una conferencia internacional sobre el Alzheimer en diciembre pasado, estaba más emocionada por el futuro que por celebrar el pasado.
Lo que emocionó a Sperling, quien ganó el premio por su trabajo en ensayos clínicos de tratamientos para el Alzheimer, fue una sensación de esperanza, que notoriamente ha faltado en la investigación de la enfermedad durante muchos años. La mayoría de los demás asistentes sintieron lo mismo.
Apenas unos meses antes de la reunión, los investigadores habían anunciado que un fármaco de anticuerpos llamado lecanemab redujo claramente la cantidad de placas de proteína amiloide (un signo revelador de la enfermedad) en los cerebros de los participantes en un ensayo clínico y ralentizó su deterioro cognitivo.
Sperling, que dirige un laboratorio en la Escuela de Medicina de Harvard en Boston, Massachusetts, estaba animada mientras agarraba el micrófono con fuerza. Después de pasar más de 30 años frustrantes en la investigación del Alzheimer, dijo, finalmente hubo pruebas de que ella y sus colegas estaban en el camino correcto. “Pero aun así, no es suficiente”, dijo.
En el ensayo, el tratamiento condujo a una reducción del 25 % del deterioro, lo suficiente como para brindarles a los participantes algunos meses más de vida independiente 1 . “Pero conquistar una enfermedad destructiva que afecta a decenas de millones de personas en todo el mundo es una historia diferente”, dice.
Además, lecanemab, comercializado en los Estados Unidos como Leqembi, constituye un régimen de tratamiento duro . Tiene que ser infundido a través de una vena por un profesional de enfermería. Y debido a que el medicamento puede causar inflamación y hemorragias cerebrales potencialmente mortales, las personas que lo toman deben ser monitoreadas regularmente.
Un anticuerpo similar, aducanumab, fue aprobado por la Administración de Drogas y Alimentos de EE.UU. en 2021 , pero la decisión generó controversia porque el ensayo clínico del fármaco no había demostrado un beneficio inequívoco.
A pesar de estas arrugas, los resultados de lecanemab consolidaron la esperanza de que la enfermedad de Alzheimer podría eventualmente prevenirse, si se administra el tratamiento lo suficientemente temprano.
El éxito también planteó otra posibilidad: este y futuros medicamentos podrían usarse en combinación para abordar diferentes etapas de la enfermedad, que a menudo están gobernadas por diferentes moléculas. Pocos esperan que una sola terapia sea la respuesta. Pero los ensayos de terapia combinada son caros y complicados, porque cada fármaco tiene que probarse tanto por sí solo como con su pareja. Las compañías farmacéuticas pueden desconfiar de unir su producto a otro, en caso de que la combinación falle y arroje una sombra sobre su medicamento.
El estado de ánimo de mayor confianza entre los que están en el campo no se debe solo al éxito de los anticuerpos antiamiloides. El armario está repleto de posibles nuevas terapias y medicamentos abandonados que ahora se están desempolvando.
Combinaciones prometedoras
La enfermedad de Alzheimer tiene un comienzo largo y silencioso. En primer lugar, las placas, grupos de proteínas beta-amiloides pegajosas, comienzan a acumularse en el cerebro. Rápidamente se rodean de células inmunitarias llamadas microglia que intentan, pero finalmente fallan, mordisquearlos. Las placas crecen en tamaño y número, pero pasan desapercibidas durante años, incluso décadas, hasta que provocan que otra proteína, llamada tau, se acumule en niveles tóxicos y se esparza por el cerebro en marañas.
Los científicos todavía están investigando exactamente cómo ocurre esta cadena de eventos, pero los síntomas cognitivos comienzan a surgir solo cuando ya está en marcha. La gravedad de los síntomas se correlaciona con la extensión de los ovillos de tau.
Hasta ahora, las terapias individuales dirigidas a tau no han funcionado bien en los ensayos 2 . Pero los científicos creen que los medicamentos que eliminan la proteína tau podrían funcionar mejor cuando se combinan con la terapia antiamiloide.
Se sabe que el amiloide de alguna manera impulsa la acumulación de tau patológica, que luego se propaga por el cerebro como un reguero de pólvora. Por ello, los científicos creen que tiene sentido eliminar la sustancia que alimenta las llamas, mientras tratan de apagar el fuego de los enredos de la tau.

Randall Bateman (izquierda) y sus colegas realizarán una prueba de anticuerpos anti-tau y anti-amiloide. Fuente: Matt Miller/Facultad de Medicina de la Universidad de Washington
Bateman y sus colegas comenzaron a planificar un ensayo de este tipo en 2015, pero se volvió factible solo recientemente, después de que surgieron los primeros indicios de que las terapias con amiloide podrían resultar efectivas. El año pasado, lanzaron una prueba internacional conocida como Tau NexGen. Están reclutando a 168 participantes, todos los cuales probablemente desarrollen la enfermedad de Alzheimer a una edad temprana, generalmente entre los 30, 40 o 50 años, porque tienen una mutación en un gen que los lleva a producir en exceso amiloide-β.
Los participantes se dividen en dos grupos , según si ya tienen síntomas de demencia o si se espera que desarrollen síntomas en los próximos diez años (estas personas suelen volverse sintomáticas aproximadamente a la misma edad que el padre del que heredaron la mutación).
Todos los participantes recibirán lecanemab y un anticuerpo reductor de tau, pero en diferentes órdenes. Aquellos sin síntomas recibirán el anticuerpo anti-tau E2814 durante un año, luego se les agregará lecanemab; el grupo sintomático recibirá lecanemab durante seis meses y luego se le agregará E2814. Los investigadores que llevan a cabo el ensayo esperan poder usar esta configuración para conocer las combinaciones óptimas de tratamiento.
Eventualmente se incluirán más medicamentos anti-tau en el estudio, y los primeros resultados del ensayo se esperan después de 2027.
Tau NexGen es el primer ensayo clínico en curso, y hasta ahora el único, de una terapia combinada para la afección. Se está planificando un ensayo 3 similar en los EE.UU. para la enfermedad de Alzheimer esporádica y de inicio tardío, que afecta a las personas mayores y representa la gran mayoría de los casos. Se espera que los Institutos Nacionales de Salud (NIH) de EE.UU. decidan en los próximos meses si cofinanciarán este esfuerzo, llamado ensayo ATP, como una asociación público-privada con compañías farmacéuticas. Si lo hace, el reclutamiento podría comenzar el próximo año.
Muchas compañías farmacéuticas y de biotecnología están desarrollando terapias anti-tau, algunas como anticuerpos, otras utilizando otras moléculas pequeñas o enfoques genéticos más nuevos para bloquear la producción de formas patológicas de tau. El colíder del ensayo ATP, Adam Boxer, neurólogo de la Universidad de California en San Francisco, dice que varias de estas empresas han expresado formalmente su interés en participar.
Al igual que Tau NexGen, este será un tipo de prueba de prevención. Los participantes tendrán pocos o ningún síntoma detectable, pero tendrán evidencia de análisis de sangre y escaneos de que sus cerebros contienen placas y signos tempranos de ovillos tau. Habrá alrededor de 900 participantes en 6 brazos, que recibirán una de las dos terapias de tau, ya sea sola o en combinación con lecanemab, lecanemab solo o un placebo.
Los equipos de investigación esperan que el tratamiento anti-tau aumente los modestos beneficios de lecanemab y que, en un círculo virtuoso, al reducir la carga de placa, lecanemab cree mejores condiciones para que funcione la terapia anti-tau.
La clave de los ensayos es una gama de nuevos biomarcadores sensibles: mediciones del cerebro o la sangre que dan una lectura del estado de la enfermedad. Los escáneres cerebrales controlan la presencia y la gravedad de las placas de amiloide y los ovillos de tau; las pruebas en sangre o líquido cefalorraquídeo miden muchas otras moléculas en la cadena de patología, como diferentes formas de amiloide y tau. Los investigadores esperan que los extensos datos moleculares y clínicos que produzcan ayuden a descubrir más sobre los mecanismos del Alzheimer.
Los ensayos de terapias combinadas tienen algunos inconvenientes: son complejos y costosos de administrar. Se estima que la prueba de ATP costará muchos cientos de millones de dólares, a pesar de los nuevos biomarcadores, que hacen que las pruebas sean mucho más eficientes.
Los anticuerpos en sí mismos constituyen terapias costosas. Lecanemab se comercializará a US$26.500 por un año de tratamiento. Aducanumab (vendido como Aduhelm en los Estados Unidos) tenía un precio original de $56,000 por un año de tratamiento, pero los fabricantes redujeron el precio a la mitad después de la protesta pública.
Los medicamentos también son inconvenientes para los pacientes porque deben infundirse cada pocas semanas. Los datos de los ensayos clínicos sugieren que se requerirá una terapia de por vida para mantener a raya el Alzheimer, dicen los expertos.
“La enfermedad parece recuperarse cuando se detienen las infusiones”, dice. Debido a que el tratamiento con anticuerpos a largo plazo no es práctico, dicen, "creemos que podría tener sentido mantener un nivel bajo de amiloide con un fármaco oral que bloquee la generación del péptido" una vez que los anticuerpos hayan eliminado las placas.
Tales compuestos existen. Alrededor de 2010, los investigadores probaron un conjunto de medicamentos orales que tenían como objetivo reducir el amiloide en el cerebro al disminuir las actividades de una de las dos enzimas, β-secretasa y γ-secretasa, que son clave para su producción. Pero todos los ensayos clínicos de estos medicamentos fracasaron 4 y el interés en ellos se secó, hasta que tuvieron una segunda oportunidad.
Otros ingredientes
En 2018, un grupo de compañías farmacéuticas acordó hacer algo inusual en su industria normalmente reservada. Decidieron compartir datos clínicos confidenciales de seis ensayos fallidos entre sí y con un grupo selecto de especialistas que habían sido reunidos por la Asociación de Alzheimer, un grupo de cabildeo por los derechos de los pacientes con sede en Chicago, Illinois.
La asociación quería aprender tanto como fuera posible de los desastrosos ensayos clínicos, cada uno de los cuales probó un inhibidor diferente de la enzima β-secretasa. Ninguno de los medicamentos había mostrado beneficio y, lo que es peor, muchos tenían efectos secundarios tóxicos, incluido, en algunos casos, un empeoramiento de la cognición. En lugar de dejar que los datos del ensayo se acumularan a puertas cerradas, la asociación quería que se discutieran en detalle. El objetivo, era "ayudar al campo a comprender más sobre las biologías relacionadas con enfermedades a las que se dirigen estos fármacos en investigación".
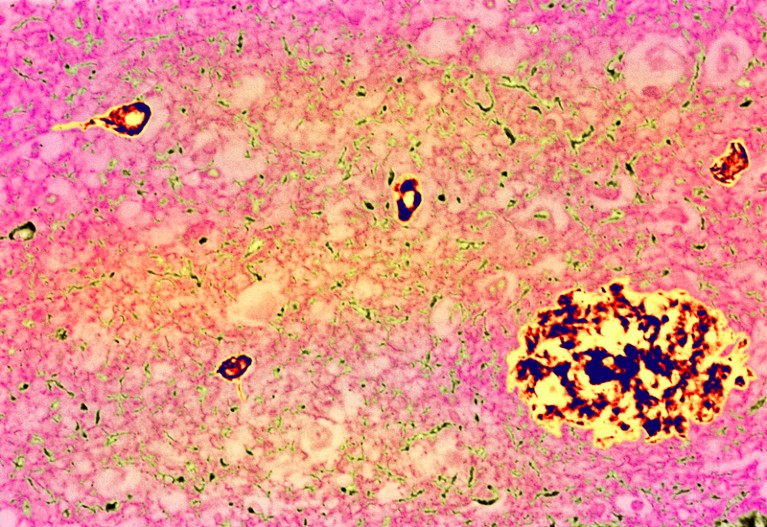
Características clásicas de la enfermedad de Alzheimer: una placa (grumos grandes) y ovillos de tau (grumos pequeños). Fuente: Simon Fraser/Science Photo Library
El artículo de revisión del panel, publicado en 2021, sugiere que la enfermedad podría haber estado demasiado avanzada en los participantes del ensayo para que esta clase de medicamento mejorara los síntomas, y que las dosis más bajas podrían evitar los efectos secundarios 5 .
Aisen cree que debería ser posible usar estos medicamentos en dosis bajas para detener la reaparición de las placas, una vez que las placas existentes se hayan eliminado con anticuerpos.
Un lote de ensayos clínicos dirigidos a la γ-secretasa también fracasó. Pero en lugar de abandonar el objetivo, los investigadores han estado trabajando en un enfoque más matizado. En lugar de bloquear por completo la enzima, una herramienta contundente que contribuye a los efectos secundarios tóxicos observados en los ensayos, esperan cambiar su comportamiento.
Uno de esos moduladores, un compuesto desarrollado en una colaboración académica 6 , se probará en un ensayo clínico inicial este año. El fármaco, que se puede tomar por vía oral, hace que la enzima corte el amiloide en proteínas más cortas, que no son tóxicas e incluso podrían ser protectoras. El ensayo será patrocinado por una nueva empresa, Acta Pharmaceuticals en Boston, Massachusetts, y financiado por los NIH.
La mayoría de los medicamentos que se están considerando para los ensayos combinados tienen como objetivo el amiloide o la proteína tau. Pero existen enfoques en etapas más tempranas que buscan mejorar los mecanismos naturales de defensa inmunológica del cerebro contra el Alzheimer. Una vez más, los investigadores han aprendido mucho de las familias con mutaciones genéticas que las predisponen a la enfermedad de Alzheimer.
La mutación en cuestión está en un gen llamado TREM2 , que produce una molécula que se asienta en la superficie de los guerreros del sistema inmunitario del cerebro, la microglía. “Afinar la microglía podría hacerla más eficiente para eliminar las placas o evitar que se propague la patología amiloide”, dice el neurocientífico Christian Haass de la Universidad Ludwig Maximilian de Munich en Alemania, “particularmente si la carga de placa se reduce primero con terapia anti-amiloide”. Está planeando experimentos en ratones para probar cómo podría funcionar un anticuerpo que se une a TREM2 y activa la microglía si se toma junto con la terapia anti-amiloide. Un anticuerpo similar se encuentra en un ensayo clínico de fase inicial como tratamiento individual.
Vacunas, genes y plasma
Más enfoques para detener el Alzheimer están llegando a los ensayos clínicos. Los investigadores tienen como objetivo llevar moléculas útiles al cerebro a través de vacunas, vectores virales o transfusiones de sangre.
Al igual que los medicamentos enzimáticos, las vacunas se están reinventando mucho después de que se detuviera el primer ensayo clínico de una vacuna antiamiloide en 2002, cuando se observó inflamación cerebral en algunos participantes.
Ahora hay varias vacunas anti-tau y anti-amiloide en preparación o en ensayos clínicos de fase inicial. Comprenden fragmentos de las proteínas tau o amiloide-β, elegidos y empaquetados para evitar respuestas inflamatorias graves. Están diseñados para estimular el sistema inmunitario del cerebro para que reconozca y destruya las versiones completas de las proteínas, y estaban destinados principalmente a prevenir enfermedades o retrasar la progresión de enfermedades tempranas. Los científicos incluso están tratando de desarrollar vacunas para atacar tanto a tau como a amiloide-β.
Otros investigadores apuestan por la terapia génica para conquistar las formas de Alzheimer causadas por mutaciones genéticas
Distintas formas del gen APOE , que codifica una proteína involucrada en el metabolismo de las grasas, afectan el riesgo de enfermedad de Alzheimer de diferentes maneras. El alelo APOE4 está relacionado con un mayor riesgo, mientras que el alelo APOE2 lo disminuye. Para su ensayo abierto, en el que todos los participantes recibieron la terapia, Lexeo Therapeutics, con sede en la ciudad de Nueva York, reclutó a 15 voluntarios con síntomas leves de Alzheimer que tienen 2 copias del gen APOE4 . Querían probar si la entrega de la variante del gen APOE2 mitigaría el efecto nocivo de la versión de mayor riesgo. Así que unieron el gen a un vector viral, que luego inyectaron directamente en el líquido cefalorraquídeo de los voluntarios.
El injerto de genes parece haber tenido éxito. Lexeo informó el año pasado que el gen APOE2 se detectó en el líquido cefalorraquídeo de algunos participantes hasta un año después de la inyección, que hasta ahora no se han observado efectos secundarios graves y que los niveles de tau de los participantes se han reducido. Es demasiado pronto para evaluar si la progresión de la enfermedad se ha desacelerado como resultado, pero los participantes serán monitoreados hasta 2028.
La terapia génica no será adecuada para todos, porque las mutaciones genéticas conocidas determinan solo una pequeña proporción de los casos de Alzheimer. Pero el concepto de terapia de reemplazo ha sido retomado por otros. La empresa Alkahest, con sede en San Carlos, California, ha realizado un pequeño ensayo clínico para comprobar si los factores de la sangre de los jóvenes podrían sustituir a los perdidos en el proceso de envejecimiento 7 .
Algunos investigadores han tenido éxito con métodos de baja tecnología. Por ejemplo, un ensayo grande cuidadosamente controlado mostró que 18 meses de ejercicio aeróbico o estiramiento detuvieron el deterioro cognitivo en personas con deterioro cognitivo leve, lo que subraya el valor de mantener un régimen de ejercicio durante el tratamiento farmacológico.
Es demasiado pronto para decir cuál de estas posibles nuevas terapias, si es que alguna, funcionará. La mayoría de los investigadores cree que el tratamiento deberá personalizarse: las personas en diferentes etapas de la enfermedad necesitarán diferentes terapias.
Referencias
1. Van Dyck, C. H. et al. N. Engl. J. Med. 388, 9–21 (2023). Artículo
2. Imbimbo, B. P., Balducci, C., Ippati, S. & Watling, M. Neural Regen. Res. 18, 117–118 (2023). Artículo
3. Aisen, P. S. et al. J. Prev. Alzheimers Dis. 8, 306–312 (2021). Artículo
4. Bazzari, F. H. & Bazzari, A. H. Molecules 27, 8823 (2022). Artículo
5. McDade, E. et al. Nature Rev. Neurol. 17, 703–714 (2021). Artículo
6. Rynearson, K. D. et al. J. Exp. Med. 218, e20202560 (2021). Artículo
7. Hannestad, J. et al. J. Alzheimers Dis. 81, 1649–1662 (2021). Artículo






























COMENTARIOS